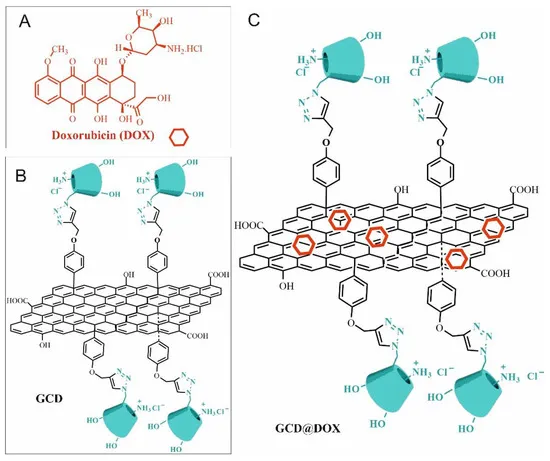
在过去十年中,纳米技术的进步为提高传统抗癌疗法的安全性和有效性带来了新的机遇。与其他载体相比,石墨烯纳米平台具有许多可调整的功能,可以装载多种生物活性化合物,尽管其生物相容性仍是一个有争议的问题。最近,我们研究了由环糊精(GCD)设计的石墨烯诱导的参与癌症相关的典型途径的基因调节。在此,我们研究了GCD对细胞安全性的影响,HEp-2对多柔比星(DOX)的反应性,以及长期暴露于GCD(GCD@DOX)上的DOX所调节的癌症相关细胞内信号通路。我们的研究证明,DOX和GCD@DOX都能诱导p53和p21信号,导致G0/G1细胞周期停滞。通过检测CDK(T14/Y15)的激活和Wee-1的表达减少,报告了DOX的遗传毒性行为。同样,我们发现DOX在接触后72小时内会裂解PARP。相反,GCD@DOX诱导了PARP的晚期裂解,这可能表明由于药物从GCD纳米载体中的可控释放而产生了较小的毒性作用。最后,自噬过程的诱导支持DOX的潜在循环,从而限制其毒性作用。这些研究结果表明,GCD@DOX是一种生物相容性药物递送系统,能够避免化疗抵抗和多柔比星的毒性。
Rosamaria Pennisi, Maria Musarra-Pizzo, Tania Velletri, Antonino Mazzaglia, Giulia Neri, Angela Scala, Anna Piperno, Maria Teresa Sciortino: Thiolated amphiphilic beta-cyclodextrin-decorated gold colloids: Synthesis, supramolecular nanoassemblies and controlled release of dopamine. Biomolecules 2022,12, 63. https://doi.org/10.3390/biom12010063


コメント