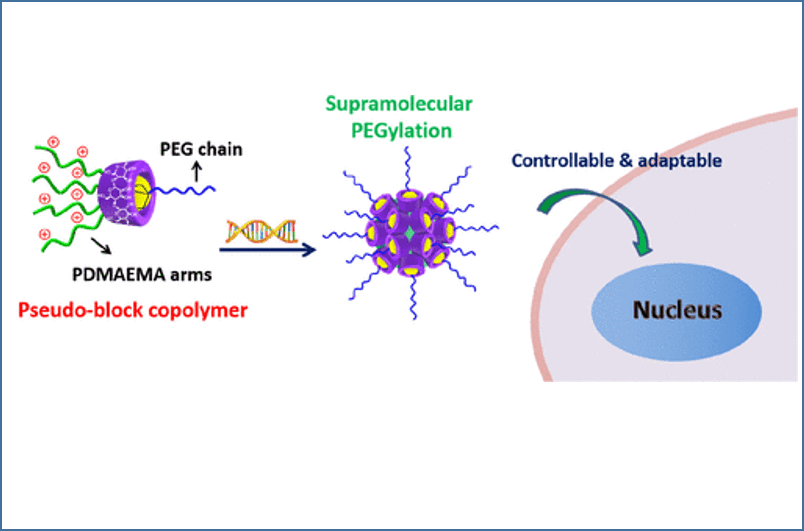
非ウイルス性のDNAデリバリーを目的として、ホスト-ゲスト型の擬ブロック共重合体を用いたカチオン性超分子システムを開発した。このシステムでは、高分子ホストは、β-シクロデキストリン(β-CD)コアとそのコアにグラフトした複数のポリ(2-(ジメチルアミノ)エチルメタクリレート)(PDMAEMA)鎖からなるカチオン性の星型ポリマーであり、高分子ゲストは、直鎖状のアダマンチルエンドのポリ(エチレングリコール)(mPEG-Ad)であった。擬ブロック共重合体は、ホストポリマーのβ-CDキャビティにゲストポリマーの末端のアダマンチル基を組み込むことにより、水性媒体中でポリマーのホストとゲストのペア(通常、1:1のモル比)から自己組織化された。このようなアプローチにより、ホストポリマーによる優れたDNA凝縮能力だけでなく、ゲストポリマーによる優れたポリプレックス安定化能力と生体適合性を兼ね備えた超分子システムが完成した。カチオン性の星型ホストポリマーだけでも、プラスミドDNAを正の表面電荷を持つナノ粒子(70~100nm)に効率よく凝縮することができた。また、L929、MB231、Helaなどの細胞株に高用量で投与したところ、PEI 25K(市販の分岐型ポリエチレンイミン、分子量約25kDa)よりも明らかに低い細胞毒性を示した。無血清または血清を含む培養条件では、これらのホストポリマーは、対象となる3つの細胞株においてPEI 25Kと比較して高いまたは低いin vitro DNAトランスフェクション効率を示し、その効率はN/P比とPDMAEMAアームの長さに依存していた。mPEG-Adとのホスト-ゲスト複合体によるPEGブロックの組み込み(すなわち、超分子PEG化)により、得られたホスト-ゲスト超分子システムは、ホストポリマー単独よりもさらに低い細胞毒性を示した。プラスミドDNA(pDNA)とホスト-ゲスト超分子システムとの間のポリプレックスは、超分子PEG化されていない対応するポリプレックスと比較して、BSA-PBS緩衝液(pH7.4)中での安定性が著しく向上し、無血清および血清含有培養条件下で、N/P比が高い場合やPDMAEMAアームが長い場合には、すべての試験対象細胞株においてin vitroのDNAトランスフェクション効率が向上した。さらに、擬ブロック共重合体を形成することで、ゲストとホストの比率を変えたり、PDMAEMAアームの長さを変えた異なるホストを使用したりすることで、超分子システムのDNAトランスフェクション能力を容易に調節・最適化することができる。
Zhongxing Zhang, Yuting Wen, Xia Song, Jingling Zhu, and Jun Li* (2021) Nonviral DNA Delivery System with Supramolecular PEGylation Formed by Host–Guest Pseudo-Block Copolymers. ACS Appl. Bio Mater.
Publication Date:June 1, 2021
https://doi.org/10.1021/acsabm.1c00306

コメント