 ドラッグデリバリー
ドラッグデリバリー シクロデキストリンとヒト多剤耐性P糖タンパク質との結合相互作用に関する計算論的モデリング
分子ドッキングと第一原理計算を組み合わせ、薬理効果が期待されるシクロデキストリン(CD:α-CD、β-CD、γ-CD)ファミリーと、薬物送達の効率化に向けた多剤耐性P-gpタンパク質の主要相互作用を初めて研究した。
 ドラッグデリバリー
ドラッグデリバリー  食品
食品  医薬品以外への応用
医薬品以外への応用 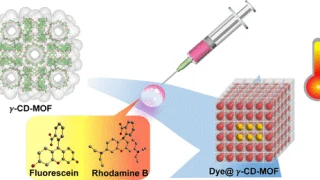 医薬品以外への応用
医薬品以外への応用  食品
食品 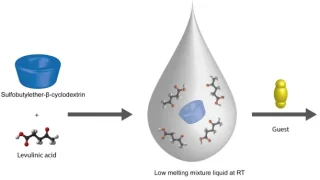 ドラッグデリバリー
ドラッグデリバリー  CD誘導体
CD誘導体  イベント
イベント  ドラッグデリバリー
ドラッグデリバリー  医薬品原薬
医薬品原薬