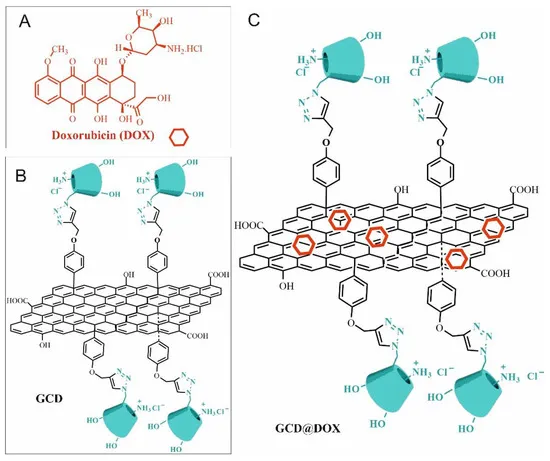
過去10年間、ナノテクノロジーの進歩は、従来の抗がん剤治療の安全性と有効性を向上させる新たな機会を生み出してきた。グラフェンナノプラットフォームは、他の担体と比較して、複数の生理活性化合物を担持するための多数の調整可能な機能性を有しているが、その生体適合性についてはまだ議論の余地がある。最近、我々は、シクロデキストリンで修飾したグラフェンによって、がん関連正常経路に関与する遺伝子のモジュレーションが誘導されることを研究した。ここでは、GCDが細胞の安全性に及ぼす影響、ドキソルビシン(DOX)に対するHEp-2の反応性、およびGCDにDOXを担持させたグラフェン(GCD@DOX)の長期曝露により変調するがん関連細胞内シグナル伝達経路について検討した。その結果、DOXとGCD@DOXの両方がp53とp21シグナルを誘導し、G0/G1細胞周期を停止させることが明らかとなった。DOX の遺伝毒性は,CDK (T14/Y15) の活性化と Wee-1 の発現低下によって検出された。同様に、曝露後72時間以内にDOXによるPARPの切断が確認された。これは、GCD ナノキャリアからの薬剤の放出が制御されているため、毒性が低いことを示している可能性がある。最後に、オートファジー過程の誘導は、DOXの潜在的なリサイクルとその結果としての毒性作用の制限を支持するものである。これらの知見は、GCD@DOXが化学療法抵抗性とドキソルビシン毒性を回避することができる生体適合性薬物送達システムであることを実証している。
Rosamaria Pennisi, Maria Musarra-Pizzo, Tania Velletri, Antonino Mazzaglia, Giulia Neri, Angela Scala, Anna Piperno, Maria Teresa Sciortino: Thiolated amphiphilic beta-cyclodextrin-decorated gold colloids: Synthesis, supramolecular nanoassemblies and controlled release of dopamine. Biomolecules 2022,12, 63. https://doi.org/10.3390/biom12010063


コメント