CNR-ISMN ナノ構造材料研究所の研究グループでは、非ステロイド性抗炎症薬ジクロフェナク(DCF)を担持したポリ-β-アミノ-シクロデキストリン(PolyCD)を基盤分子とする超分子相互作用で連結したナノアセンブリーを開発した。
非ステロイド性抗炎症薬ジクロフェナク(DCF)を担持したポリ-β-アミノシクロデキストリン(PolyCD)を基盤とし、蛍光プローブ(アダマンタニル-ローダミン結合体、Ada-Rhod)と超分子相互作用で連結したナノアセンブリーが、骨関節疾患の炎症管理のために開発された。
また、ポリCD@Ada-Rhod/DCFは、hMSCにおけるIL-1産生を有意に抑制し、これらのナノ集合体の抗炎症作用が示された。[1]
フルオレセインイソチオシアネート(FITC)を担持した両親媒性カチオン性β-シクロデキストリン(ambCD) ナノベシクルのリソグラフィー的に制御された濡れ性(LCW)を用いて、ambCD/FITCを幾何学的に作製した。これは、機能化された表面を用いて、細胞環境のマルチスケール制御を実現している。ambCDの 官能化は、その素地となる基質の表面エネルギーに強く影響された。疎水性に応じて、異なる方法でambCDを配向させることで、細胞に対して異なる作用を誘導することが示された。
ヒト神経芽細胞腫SHSY5Y細胞において、細胞誘導とaCD/FITC細胞の内在化が実証された [2]。
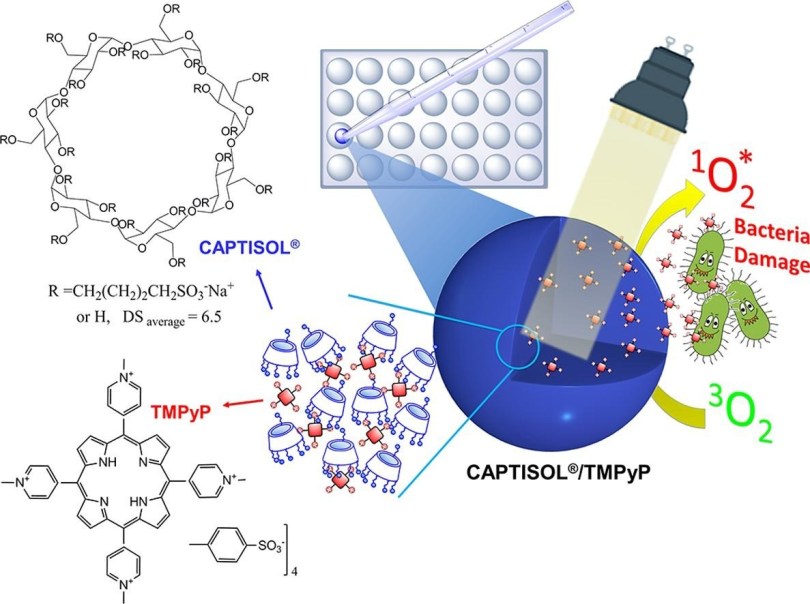
抗菌性光線力学的治療(aPDT)のための効率的な生体適合性システムを構築するために、市販のシクロデキストリンCAPTISOL®(スルホブチルエーテルβ-シクロデキストリン、SBE-β-CD)と5,10,15,20-テトラキス(1-メチルピリジニウム-4-イル)ポルフィンテトラキス(p-トルエンスルホン酸)(TMPyP)をベースとした新規ナノ光治療薬が設計された。生理的条件下での放出および光安定性の研究が行われ、ポルフィリンの放出を2週間以上持続させ、光分解からPSを保護するCAPTISOL®の役割が指摘されている。グラム陰性P. aeruginosa、大腸菌、グラム陽性S. aureusに対するナノアセンブリーと遊離ポルフィリンの光抗菌活性は、遊離TMPyPよりも高く、ナノアセンブリーは放出持続性と高い光安定性を示し、作用部位でのPDT効果が最適化された。[3]
アシル鎖長が4個(ACyD4)と8個(ACyD8)のメデューサ様ACyDと、1次側をチオヘキシル、2次側をオリゴエチレン(SC6OH)で修飾したブーケ様CyDの2つのメデューサ様ACyDを、ナノ構造への集合体化能力、またはジパルミトイルホスファチジルコリン(DPPC)/ACyDsのハイブリッドシステムを形成する能力について調べた。最も短いメデューサ様ACyD4を除いて、他のACyDsは少なくとも45日間安定なナノアグリゲートを形成した。また、ACyDsのDPPCリポソームの熱物性への影響を示差走査熱量分析によって調べたところ、リポソームとACyDsの相互作用が明らかになり、リポソーム/ACyDsのハイブリッドシステムが得られた。[4]
シクロデキストリン(CD)で装飾され、ドキソルビシン(DOX)を担持したグラフェン(G)の細胞内動態と、がん関連の標準的な経路に関与する遺伝子の変調を研究した。FLIM、ラマンマッピングおよび蛍光顕微鏡によって追跡されたGCD@DOXの細胞内運命は、GCD@DOXの効率的な細胞内取り込みおよびグラフェン担体非存在下において核内にDOXの存在が確認された。GCD単独(25 μg/mL)で処理した細胞は、16の遺伝子発現に変化が認められた。全体として、14の一般的な遺伝子がGCDとGCD@DOXで処理した細胞の両方で異なる発現を示し、これらの遺伝子のうち4つは反対の傾向を示した。また、安全で効果的なグラフェンベースの薬物/遺伝子送達システムを合理的に設計するためには、亜細胞毒性を示すグラフェン濃度でも癌関連遺伝子の修飾を考慮する必要がある[5]。

[1] Cordaro, A., Zagami, R., Malanga, M., (…), Piperno, A., Mazzaglia, A. (2020) Cyclodextrin cationic polymer-based nanoassemblies to manage inflammation by intra-articular delivery strategies Nanomaterials 10(9),1712. https://doi.org/10.3390/nano10091712
[2] Valle, F., Tortorella, S., Scala, A., (…), Biscarini, F., Mazzaglia, A. (2020) Amphiphilic cationic cyclodextrin nanovesicles: A versatile cue for guiding cell adhesion. Nanoscale Advances 2(12), pp. 5897-5904. https://doi.org/10.1039/D0NA00623H
[3] Zagami, R., Franco, D., Pipkin, J.D., (…), Monsù Scolaro, L., Mazzaglia, A. (2020) Sulfobutylether-β-cyclodextrin/5,10,15,20-tetrakis(1-methylpyridinium-4-yl)porphine nanoassemblies with sustained antimicrobial phototherapeutic action. International Journal of Pharmaceutics 585,119487. https://doi.org/10.1016/j.ijpharm.2020.119487
[4] Musumeci, T., Bonaccorso, A., De Gaetano, F., (…), Puglisi, G., Ventura, C.A. (2020) A physico-chemical study on amphiphilic cyclodextrin/liposomes nanoassemblies with drug carrier potential. Journal of Liposome Research 30(4), pp. 407-416. https://doi.org/10.1080/08982104.2019.1682603
[5] Caccamo, D., Currò, M., Ientile, R., (…), Piperno, A., Sciortino, M.T. 2020Intracellular fate and impact on gene expression of doxorubicin/cyclodextrin-graphene nanomaterials at sub-toxic concentration. International Journal of Molecular Sciences 21(14),4891, pp. 1-19 https://doi.org/10.3390/ijms21144891



コメント